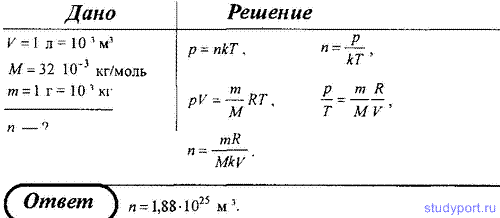
Отношение числа молекул газа к его объему
Объемный и массовый расход газа
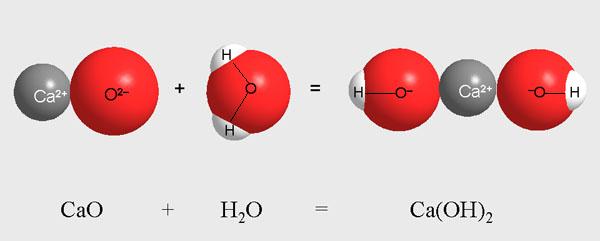
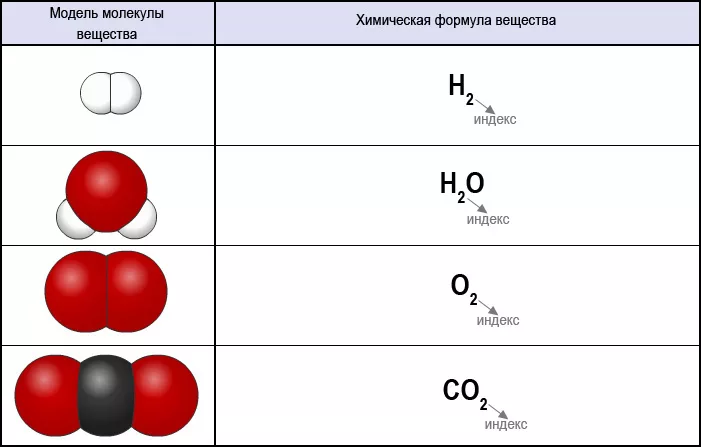
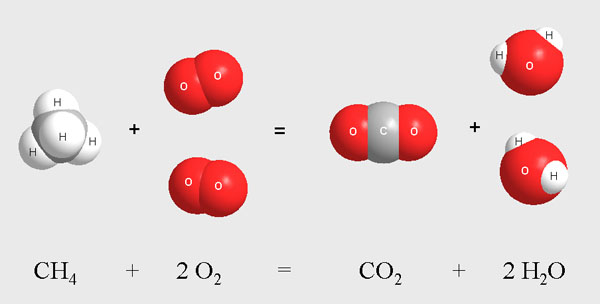
Для того чтобы лучше понимать термин «Молярный объем газа», вспомним что такое газы и газовые законы. То есть мы понимаем, что большое количество частиц с большой скоростью располагается в пространстве. Что будет, если мы ограничим это пространство? В этом объеме будет помещаться определенное количество частиц газа, ведь мы просто ограничили пространство, в котором эти частицы располагаются. Что будет, если мы поменяем эти частицы качественно — допустим, заменим водород на кислород?

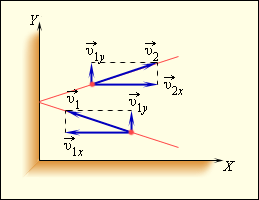





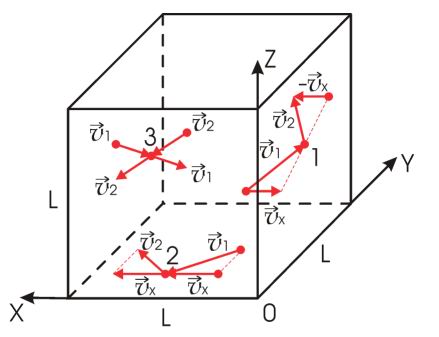
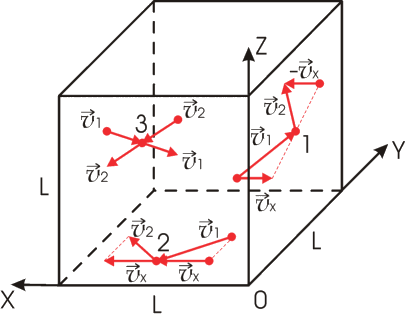
Связь температуры газа со средней кинетической энергией поступательного теплового движения его частиц. Доказательство теоремы. Вывод формулы : используя модель идеального газа, предполагается, что давление газа на стенки сосуда возникает в результате ударов отдельных молекул. Применено приближение: поскольку молекул в кубе достаточно много, то какой бы маленький объем внутри куба мы ни взяли, всегда найдется молекула с координатой внутри этого объема, летящая вдоль выбранного направления со скоростью v. Значит, можно рассчитать время полета молекулы между стенками, как будто это одна молекула летает между стенками без столкновений с другими молекулами. Разные молекулы, движущиеся с различными скоростями v 1 , v 2 , v 3 , … создадут суммарную силу удара:.
- Идеальный газ - математическая модель газа, в которой предполагается, что потенциальной энергией молекул можно пренебречь по сравнению с их кинетической энергией.
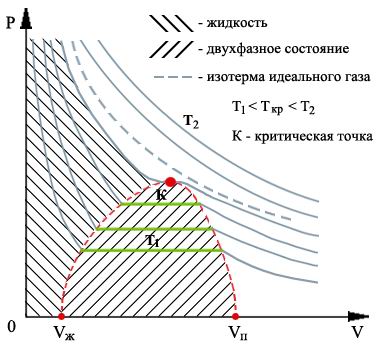
- Газы часто используются в тепловых двигателях в качестве рабочего тела. Это обусловлено их свойством менять объем в широком диапазоне, и, следовательно, получать работу расширения.
- Основы вакуумной техники.
- В г.
- Основные термины, применяемые в вакуумной технике, соответствуют ГОСТ ; и
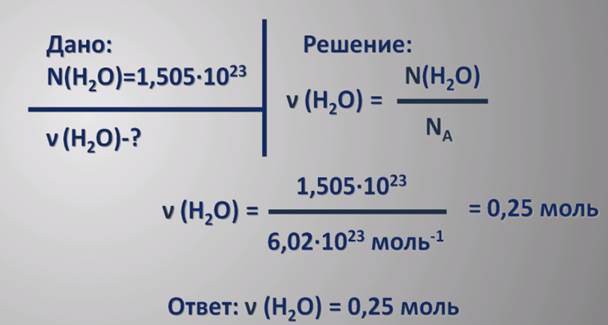
- Выразим массу каждого газа через количество вещества и молярную массу:.
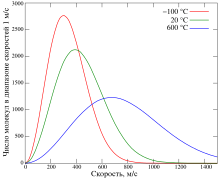





Исходя из определения идеального газа, в нем отсутствует потенциальная составляющая внутренней энергии отсутствуют силы взаимодействия молекул, кроме ударного. Таким образом, внутренняя энергия идеального газа представляет собой только кинетическую энергию движения его молекул. Ранее уравнение 2.






